对比法在化学教学中的应用
对比法在化学教学中的应用
作者/ 韩 尚
对比法是根据一定的标准对某类现象在不同情况的不同表现进行比较的一种研究方法。运用对比法,可以更为准确地理解事物的本质特征,区分相近事物,把握事物之间的内在联系及其变化规律,是学习化学过程中不可缺少的方法。在化学教学中,对一些概念、反应原理、实验、计算,运用对比法进行教学,可以帮助学生开拓思维,加深理解,便于掌握和应用。
一、对比使概念的学习变得简单直观
有些同学在化学学习中对于物质的分类不是很清楚,常把含有不同元素的纯净物划分到混合物中,混淆了纯净物和混合物、单质和化合物的划分的标准,所以化学概念中有些字词,既是理解概念的关键点,也是与易混概念的区别点。为了帮助学生能够对纯净物和混合物进行判断,并加深对单质和化合物的认识,我做了以下比较:物质可根据组成物质的种类多少分成纯净物和混合物,而纯净物和混合物的主要区别是有无固定的熔、沸点,纯净物有固定的熔、沸点,混合物如空气、溶液、矿石没有固定的熔、沸点,就纯净物来说根据组成物质中元素种类多少又可分成单质和化合物,而单质又可分为金属单质、非金属单质、稀有气体,化合物包括氧化物等。在这里学生要重点弄清,元素可以组成单质和化合物,而单质不能组成化合物。
二、运用对比使化学反应原理变得清晰
学习碱的性质时,常见的碱能和二氧化碳反应,二氧化碳通入澄清石灰水,澄清石灰水会变浑浊证明有新物质生成,发生了化学变化;但将二氧化碳通入氢氧化钠溶液,我们知道是发生了化学变化,没有现象怎能使学生明白呢?于是我又设计了以下的实验:用两个干燥的塑胶瓶收集满二氧化碳,然后往这两个瓶分别倒入等体积水和氢氧化钠溶液,盖上瓶盖,再振荡,通过观察发现两个塑胶瓶都变瘪了,为什么变瘪的程度会不同呢?最后,引导学生对实验过程和实验现象进行讨论与总结,装有水的塑胶瓶只是瘪了一半,是由于二氧化碳能溶于水,使瓶内的气体减少而瓶内压强小于大气压故瓶变瘪;而装有氢氧化钠溶液的塑胶瓶就完全变瘪了,是因为不仅氢氧化钠溶液中的溶剂水能溶解二氧化碳,还有是溶质氢氧化钠能和二氧化碳反应。通过所设计的对比实验不但复习了旧的知识(二氧化碳的水溶性),还能掌握新的知识(二氧化碳能和氢氧化钠反应)。这样,就使学生在实验中既培养了基本技能和科学方法,又提升了知识水平和思维能力,受益匪浅。
三、运用对比使化学计算的思路更广阔
例题:有炭粉和氧化铜的黑色固体混合物20g,加强热后将生成的气体通入足量的石灰水中,气体被完全吸收,产生了10g沉淀,求原混合物中炭的质量?
解法一:化学方程式法。
学生的习惯思维是:看完题后,直接写出化学方程式Ca(OH)2+CO2=CaCO3↓+H2O。根据CaCO3的质量求出CO2的质量是4.4克,再根据
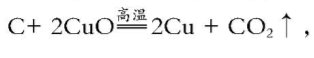
求得碳的质量是1.2g。
解法二:质量守恒定理法。
根据上述两个反应可知,在解题过程中,C——CO2——CaCO3中碳元素的质量没有改变,那么CaCO3中的碳元素的质量=10g*12/100=1.2g就是我们所求解炭粉的质量。
通过上述两个解题方法的比较,第一种方法学生能很快解决,思路也清晰,但计算烦琐;第二种方法简单,但学生们想到的几乎没有,能做出需要有较深的功底。同学们可以从这两个解题的方法中悟出:化学方程式的计算如果太复杂了,可以转换思维运用质量守恒定理来求解。在化学计算中如果能够巧妙在运用守恒的思想,往往能够避繁就简,取得事半功倍的效果。
四、运用对比有利于学生确定实验方案
在学习二氧化碳实验室制取这一节内容时,教科书上没有设计对比试验,直接就给了实验室制取二氧化碳用的是稀盐酸和石灰石,如果教师照本宣科,学生虽然知道了用什么药品可以制取二氧化碳,但不知道为什么要选取稀盐酸和石灰石来制取,而不用其他的酸或其他药品制取呢?此时可以设计这样一组对比实验。实验一:石灰石+稀硫酸,观察现象。实验二:碳酸钠+稀盐酸,观察现象。实验三:碳酸钠+稀硫酸,观察现象。实验四:石灰石+稀盐酸,观察现象。
学生观察到:实验一反应速率太慢,一会儿就停止;实验二、实验三反应速率太快,不利于收集气体;只有实验四反应速度适中,且能持续进行,有利于气体的收集,适合实验室制取。通过四个实验的对比,引导学生从不同的反应中找出适合实验室制取CO2的药品是石灰石与稀盐酸,并通过观察、分析,最终确定了实验方案。
总之,在化学教学中应用对比法,不仅使学生对所学知识更加深刻而牢固,而且使学生获取的新知识更加鲜明准确。
(河北省晋州市第七中学) 《对比法在化学教学中的应用》
本文链接地址:http://www.oyaya.net/fanwen/view/60975.html
作者/ 韩 尚
对比法是根据一定的标准对某类现象在不同情况的不同表现进行比较的一种研究方法。运用对比法,可以更为准确地理解事物的本质特征,区分相近事物,把握事物之间的内在联系及其变化规律,是学习化学过程中不可缺少的方法。在化学教学中,对一些概念、反应原理、实验、计算,运用对比法进行教学,可以帮助学生开拓思维,加深理解,便于掌握和应用。
一、对比使概念的学习变得简单直观
有些同学在化学学习中对于物质的分类不是很清楚,常把含有不同元素的纯净物划分到混合物中,混淆了纯净物和混合物、单质和化合物的划分的标准,所以化学概念中有些字词,既是理解概念的关键点,也是与易混概念的区别点。为了帮助学生能够对纯净物和混合物进行判断,并加深对单质和化合物的认识,我做了以下比较:物质可根据组成物质的种类多少分成纯净物和混合物,而纯净物和混合物的主要区别是有无固定的熔、沸点,纯净物有固定的熔、沸点,混合物如空气、溶液、矿石没有固定的熔、沸点,就纯净物来说根据组成物质中元素种类多少又可分成单质和化合物,而单质又可分为金属单质、非金属单质、稀有气体,化合物包括氧化物等。在这里学生要重点弄清,元素可以组成单质和化合物,而单质不能组成化合物。
二、运用对比使化学反应原理变得清晰
学习碱的性质时,常见的碱能和二氧化碳反应,二氧化碳通入澄清石灰水,澄清石灰水会变浑浊证明有新物质生成,发生了化学变化;但将二氧化碳通入氢氧化钠溶液,我们知道是发生了化学变化,没有现象怎能使学生明白呢?于是我又设计了以下的实验:用两个干燥的塑胶瓶收集满二氧化碳,然后往这两个瓶分别倒入等体积水和氢氧化钠溶液,盖上瓶盖,再振荡,通过观察发现两个塑胶瓶都变瘪了,为什么变瘪的程度会不同呢?最后,引导学生对实验过程和实验现象进行讨论与总结,装有水的塑胶瓶只是瘪了一半,是由于二氧化碳能溶于水,使瓶内的气体减少而瓶内压强小于大气压故瓶变瘪;而装有氢氧化钠溶液的塑胶瓶就完全变瘪了,是因为不仅氢氧化钠溶液中的溶剂水能溶解二氧化碳,还有是溶质氢氧化钠能和二氧化碳反应。通过所设计的对比实验不但复习了旧的知识(二氧化碳的水溶性),还能掌握新的知识(二氧化碳能和氢氧化钠反应)。这样,就使学生在实验中既培养了基本技能和科学方法,又提升了知识水平和思维能力,受益匪浅。
三、运用对比使化学计算的思路更广阔
例题:有炭粉和氧化铜的黑色固体混合物20g,加强热后将生成的气体通入足量的石灰水中,气体被完全吸收,产生了10g沉淀,求原混合物中炭的质量?
解法一:化学方程式法。
学生的习惯思维是:看完题后,直接写出化学方程式Ca(OH)2+CO2=CaCO3↓+H2O。根据CaCO3的质量求出CO2的质量是4.4克,再根据
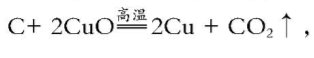
求得碳的质量是1.2g。
解法二:质量守恒定理法。
根据上述两个反应可知,在解题过程中,C——CO2——CaCO3中碳元素的质量没有改变,那么CaCO3中的碳元素的质量=10g*12/100=1.2g就是我们所求解炭粉的质量。
通过上述两个解题方法的比较,第一种方法学生能很快解决,思路也清晰,但计算烦琐;第二种方法简单,但学生们想到的几乎没有,能做出需要有较深的功底。同学们可以从这两个解题的方法中悟出:化学方程式的计算如果太复杂了,可以转换思维运用质量守恒定理来求解。在化学计算中如果能够巧妙在运用守恒的思想,往往能够避繁就简,取得事半功倍的效果。
四、运用对比有利于学生确定实验方案
在学习二氧化碳实验室制取这一节内容时,教科书上没有设计对比试验,直接就给了实验室制取二氧化碳用的是稀盐酸和石灰石,如果教师照本宣科,学生虽然知道了用什么药品可以制取二氧化碳,但不知道为什么要选取稀盐酸和石灰石来制取,而不用其他的酸或其他药品制取呢?此时可以设计这样一组对比实验。实验一:石灰石+稀硫酸,观察现象。实验二:碳酸钠+稀盐酸,观察现象。实验三:碳酸钠+稀硫酸,观察现象。实验四:石灰石+稀盐酸,观察现象。
学生观察到:实验一反应速率太慢,一会儿就停止;实验二、实验三反应速率太快,不利于收集气体;只有实验四反应速度适中,且能持续进行,有利于气体的收集,适合实验室制取。通过四个实验的对比,引导学生从不同的反应中找出适合实验室制取CO2的药品是石灰石与稀盐酸,并通过观察、分析,最终确定了实验方案。
总之,在化学教学中应用对比法,不仅使学生对所学知识更加深刻而牢固,而且使学生获取的新知识更加鲜明准确。
(河北省晋州市第七中学) 《对比法在化学教学中的应用》

 ★读了本文的人也读了:
★读了本文的人也读了: